Latvijā iedzīvotāju mūža ilgums ir otrais īsākais Eiropā. Tas raksturo valsts nodrošinātās veselības aprūpes efektivitāti. Statīnus iesaka biežākā mirstības iemesla – sirds un asinsvadu slimību – profilaksei un ārstēšanai. Diemžēl dati arī par šo medikamentu reālo efektivitāti pacientiem ir grūti pieejami, raksta iniciatīvas "Uzrādīt zāļu efektivitāti!" autors un ārsts Artis Žeigurs. Šī ir otrā no divām A. Žeigura sagatavotajām publikācijām. Pirmajā publikācijā viņš analizēja antidepresantu efektivitātes datu nepietiekamo pieejamību pacientiem. Lūdzam apsvērt atbalstu tematiski saistītajai iniciatīvai "Uzrādīt zāļu efektivitāti"! Ja atbalsti šo iniciatīvu, lūdzam ar to dalīties arī ar citiem. A. Žeigurs ir lūdzis Nacionālo Veselības dienestu (NVD) uzrādīt maz efektīvo statīnu grupas medikamentu izmaksu efektivitātes aprēķinu un ir saņēmis atbildi, "ka informācija diemžēl ir konfidenciāla un nav nododama trešajām pusēm. Pie tam jāaatzīmē, ka pirmie statīnus saturošie medikamenti tika iekļauti Kompensējamo zāļu sarakstā jau no 1999. gada.'' Par statīnu grupas medikamentiem valsts ar apšaubāmu lietderību un bez iespējām to pārbaudīt, pa šiem gadiem ir iztērējusi vairāk kā 10 miljonus veselības aprūpes naudas. Saskaņā ar NVD komentāru, pilsoniskā sabiedrība par šo līdzekļu izlietojuma lietderību tāpat kā par šo medikamentu reālo efektivitāti pārliecināties nevar. Cik procentiem lietotāju statīni mazina mirstību? No 100 pacientiem, kam ārsts ieteiks statīnus, tie mazinās mirstību tikai vienam vai diviem. Jūs taču negribētu, ka jums vai jūsu radiem iesaka zāles ar tik zemu efektivitāti un neiesaka alternatīvu? Piemēram, simvastatīna pētījumā Heart Protection Study (HPS) ir pētīti 20’500 pacientu. Zāļu lietošana pierādīti mazināja koronāru nāvi 1,2% simvastatīna lietotāju. ''1,2%'' ir absolūtais mirstības riska mazinājums jeb to zāļu lietotāju skaits procentos, kam zāles mazina mirstību, salīdzinot ar placebo. To rēķina no mirstības placebo grupā atņemot mirstību zāļu grupā (6,9-5,7=1,2).
Statīnu zemā efektivitāte. Kāpēc, izglītojot ārstus tā būtu jāuzrāda? Šobrīd kardiologu lekcijās un vadlīnijās ārstu izglītotāji neuzrāda cik procentiem lietotāju ieteiktā terapija palīdz. Ārsti neuzzina, ka zāles palīdz tikai nedaudziem lietotājiem. Tāpēc lielākajai pacientu daļai, kam zāles nelīdzēs, viņi laicīgi neiesaka citu ārstēšanu. Pacienti, dzerot zāles, cer dzīvot ilgāk un pieņem, ka ārstu ieteiktās zāles tiešām palīdzēs. Ja ārsts izraksta mazefektīvas zāles un pacientu par to nebrīdina, viņš pacietnu krāpj. Vēl par statīnu (ne)efektivitāti Koronārās nāves biežums piecu gadu ilgas simvastatīna 40 mg/d lietošanas rezultātā samazinājās par 18%, liecinja šis pats pētījums. ''Par 18%'' ir relatīvais, salīdzinošais mirstības riska mazinājums tiem, kam zāles palīdz. Bet – tas neparāda, cik procentiem lietotāju zāles palīdz! Tiem, kam zāles nepalīdz, riski, saprotams, nemazinās. Relatīvo riska mazinājumu uzsver mazefektīvo zāļu ražotāji, ja tas ir lielāks skaitlis, tāpēc, lasot zāļu aprakstus, meklējiet norādes, cik procentiem lietojāju zāles mazina mirstību, nevis par cik procentiem mazinās mirstības risks. Pravastatīna pētījums West of Scotland Coronary Prevention Study (WOSCOPS) 6500 pacienti 4,8 gadus saņēma 40 mg pravastatīnu vai placebo. Mirstības risks no koronārās sirds slimības un neletāla miokarda infarkta mazinājās 2,4% zāļu lietotāju. Pētījumā Long-Term Intervention with Pravastatin in Ischemic Disease (LIPID) 9000 pacientu 5,6 gadus saņēma 40 mg pravastatīnu. Mirstība no koronārās sirds slimības mazinājās 1,1% zāļu lietotāju.(7*) Pētījums Intervention Trial Evaluating Rosuvastatin (JUPITER). 17’800 dalībnieki.(2*) Rosuvastatīns 20 mg pieaugušajiem, mazinot holesterīnu par 45%, novērsa kardiovaskulārus notikumus mazāk nekā 1% lietotāju gadā – 0,88% lietotāju; augsta riska apakšgrupā – 0,51%. Šo zāļu lietošana jebkuru nāvi novērsa 0,25% procentiem lietotāju gadā. 400 pacienti gadu dzēra šīs zāles; mirstība mazinājās tikai vienam. 10’000 dalībnieku 3,3 gadus saņēma 10 mg atorvastatīnu angļu-skandināvu kardiālo rezultātu pētījuma lipīdu līmeņa pazemināšanas atzarā (ASCOT-LLA − Anglo-Scandinavian Cardiac Outcomes Trial Lipid Lowering Arm). Kardiovaskulāro notikumu riski mazinājās 1,9% zāļu lietotāju. 3,9 gadus ilgs 10 mg atorvastatīna pētījums 2800 diabēta pacientiem (CARDS − Collaborative Atorvastatin Diabetes Study). Nozīmīgi kardiovaskulārie notikumi (fatāli un nefatāli akūti miokarda infarkti, latenti miokarda infarkti, akūta koronāra nāve, nestabilā stenokardija, koronāro artēriju šuntēšana, perkutānā transluminālā koronārā angioplastija, revaskularizācijas, insulti) mazinājās 3,2% lietotāju. Autori gan nav uzrādījuši cik procentiem lietotāju mazinājās kopējā mirstība. Viņi tikai brīdina, ka kopējā mirstība mazinās nenozīmīgi, un to ir svarīgi ņemt vērā, izvēloties terapiju.(8*) Kāpēc, izglītojot kolēģus, ir tik svarīgi uzrādīt, cik procentiem lietotāju mazinās kopējā mirstība? Zāles mazina holesterīnu lielākajai daļai zāļu lietotāju, bet kardiovaskulāra mirstība un kopējā mirstība mazinās tikai niecīgai daļai zāļu lietotāju, ja devas ir mazas. Ja zāļu devas ir lielas, tad kardiovaskulāri notikumi mazinās, bet kopējā mirstība ne tikai nemazinās, bet pat pieaug. Tie, kuri dzēra atorvastatīnu lielās devās, mira biežāk par tiem, kas zāles nedzēra. 80 mg atorvastatīns mazina išēmiskos insultus, bet palielina hemorāģiskos insultus un kopējo mirstību, par ko kolēģi un pacienti būtu jābrīdina. Pētījums "Insulta novēršana ar holesterīna līmeņa agresīvu pazemināšanu" (SPARCL) 4'700 pacienti, 4,9 gadu ilgs pētījums.(3*) Kopējā mirstība palielinās 0,2% (9,1-8,9) atrorvastatīna lietotāju. Pacientu apakšgrupā ar agrāk pārciestu hemorāģisko insultu atorvastatīna lietošana palielināja mirstību 5,2% zāļu lietotāju. Katrs zema blīvuma lipoproteīdu holesterīna pazeminājums par milimolu litrā palielina hemorāģiska insulta iespēju par 21%.(4*) Vai statīnu devas palielināšana mazina kardiovaskulāros notikumus? Pieņēmumu 6,7 gadus pētīja, iesaistot 12‘000 pacientus, Study of the Effectiveness of Additional Reductions in Cholesterol and Homocysteine (pētījums par efektivitāti, lai vēl vairāk pazeminātu holesterīna un homocisteīna līmeni) jeb “SEARCH”. Lielākas devas nedeva labākus riska mazinājumus; nopietnu blakusefektu biežums tikai pieauga. Nozīmīgus asinsvadu sistēmas notikumus pārcieta katrs ceturtais zāļu lietotājs. 20 un 80 mg simvastatīna nozīmīgus asinsvadu sistēmas notikumus ietekmēja vienādi. 80 mg grupā 1% lietotāju cieta no miopātijas, bet 20 mg grupā tādu bija 0,2% lietotāju.(5*) Vai SATURN pētījums pierāda, ka, intensīvi lietojot statīnus, mazinās arī kardiovaskulāro notikumu skaits un mazinās pacientu mirstība? Nē, nepierāda. Skatīt – SATURN jeb The Study of Coronary Atheroma by Intravascular Ultrasound: Effect of Rosuvastatin 40 mg versus Atorvastatin 80 mg, sponsors AstraZeneca Pharmaceuticals.(6*) 1039 patients, pētījuma ilgums – viens gads un seši mēneši. SATURN nepētīja, vai intervence mazina kardiovaskulāros notikumus un kopējo mirstību. Pētnieki atzīst, ka intravaskulāra ultrasonoskopija ir surogāts mērķis, un pangas tilpuma samazinājums par simtdaļu negarantē klīnisku ieguvumu. Vienai trešdaļai pacientu slimība progresēja, neskatoties uz maksimāli intensīvu statīnu terapiju. 7% zāļu lietotāju pārcieta pirmo nopietno kardiovaskulāro notikumu mūžā. Katrs piektais pacients jeb 20% terapiju pārtrauca. Smagu blakņu dēļ atorvastatīna grupā terapiju pārtrauca 7%, rosuvastatīna grupā – 6,5%.
Lai gan klīniskajos pētījumos holesterīns mazinājās lielai statīnu lietotāju daļai, tomēr kardiovaskulārie notikumi un mirstība mazinājās tikai ap 2% zāļu lietotāju. Ja holesterīna mazināšana ar statīniem efektīvi mazinātu kardiovaskulāro notikumu riskus un pacientu mirstību, tad visiem, kam pazeminās holesterīns, būtu jāmazinās arī mirstībai, tomēr tā nenotiek. Atorvastatīna lielu devu gadījumā kopējā mirstība nemazinās vai pat pieaug. Ilgstoši lietojot lielākas statīnu devas, tās nemazina kardiovaskulāros notikumus labāk par mazām devām. Lielāku devu lietošana izraisa vairāk blakņu un palielina mirstību. Aknu fermentu bloķēšana ar statīniem nav veselīgs veids, kā mazināt holesterīnu. Tas ir arī mazefektīvs veids, kā mazināt kardiovaskulāros riskus un pacientu mirstību. Zinot statīnu zemo efektivitāti, kolēģus un pacientus vajadzētu informēt par alternatīvu, kas ir efektīvāka un veselīgāka. Piemēram, 10 tūkstošu soļu noiešana dienā.(9*) Atsauces (1*) Simvastatīna zāļu apraksts. Sirds aizsardzības pētījumā (HPS – Heart Protection Study) simvastatīna terapijas ietekmi novērtēja 20'536 pacientiem (40–80 g.v.) ar hiperlipidēmiju vai bez tās un ar koronāro sirds slimību, citu okluzīvu artēriju slimību vai cukura diabētu. Šajā pētījumā 10'269 pacientus ārstēja ar 40 mg simvastatīna dienā un 10'267 pacientus – ar placebo vidēji piecus gadus. Sākotnēji 6'793 pacientiem (33%) ZBL-H līmenis bija <116 mg/dl; 5'063 pacientiem (25%) līmenis bija 116–135 mg/dl; un 8'680 pacientiem (42%) līmenis pārsniedza 135 mg/dl. Ārstēšana ar simvastatīnu 40 mg/dienā salīdzinājumā ar placebo nozīmīgi samazināja visu iemeslu mirstības risku 12,9% (1'328) ar simvastatīnu ārstētiem pacientiem, salīdzinot ar 14,7% (1'507) pacientiem, kuri lietoja placebo (p=0,0003). Sakarā ar koronārās nāves biežuma samazināšanos par 18% (587 [5,7%] pret 707 [6,9%]; p=0,0005) absolūtā riska samazinājums ir 1,2%. (2*) Rosuvastatīna zāļu apraksts. Pētījumā Intervention Trial Evaluating Rosuvastatin (JUPITER) rosuvastatīna ietekmi uz galveno aterosklerotisko kardiovaskulāro slimību rašanos vērtēja 17'802 vīriešiem (≥50 gadus veciem) un sievietēm (≥60 gadus vecām). Pētījuma dalībnieki tika randomizēti saņemt placebo (n=8901) vai rosuvastatīnu 20 mg reizi dienā (n=8901) un tika novēroti divus gadus. Rosuvastatīna grupā ZBL holesterīna līmenis pazeminājās par 45% (p<0,001), salīdzinot ar placebo grupu. Post-hoc analīzē augsta riska apakšgrupas pacientiem ar Framingema risku <20% (1558 pacienti) novēroja ievērojamu kardiovaskulārās nāves, insulta un miokarda infarkta kombinēta galaiznākuma samazināšanos rosuvastatīna terapijas rezultātā, salīdzinot ar placebo (p=0,028). Absolūtā riska samazināšanās pret notikumu biežumu uz 1000 pacientgadiem bija 8.8. Kopējā mirstība šajā augsta riska grupā bija nemainīga (p=0,193). Post-hoc analīzē augsta riska apakšgrupas pacientiem ar sākotnējo SCORE risku ≥5% (ekstrapolēti iekļaujamie pacienti virs 65 gadiem) novēroja ievērojamu kardiovaskulārās nāves, insulta un miokarda infarkta kombinēta gala iznākuma samazināšanos rosuvastatīna terapijas rezultātā, salīdzinot ar placebo (p=0,0003). Absolūtā riska samazināšanās pret notikumu biežumu uz 1000 pacientgadiem bija 5,1. Kopējā mirstība šajā augsta riska grupā bija nemainīga (p=0,076). (3*) Atorvastatīna zāļu apraksts. Pētījumā "Insulta novēršana ar holesterīna līmeņa agresīvu pazemināšanu" (SPARCL) novērtēts 80 mg atorvastatīna vai placebo efekts 4'731 pacientam bez koronārās sirds slimības anamnēzē, kuri pēdējo sešu mēnešu laikā pārcietuši insultu vai tranzitoru išēmisku lēkmi (TIL). 60% no viņiem bija vīrieši, pacienti bija vecumā no 21−92 gadiem (vidējais vecums – 63 gadi), un ZBL līmenis pētījuma sākumā vidēji bija 133 mg/dl (3,4 mmol/l). Vidējais ZBL-H, saņemot atorvastatīnu, bija 73 mg/dl (1,9 mmol/l), bet, lietojot placebo – 129 mg/dl (3,3 mmol/l). Vidējais novērošanas laiks bija 4,9 gadi. 80 mg atorvastatīna, salīdzinot ar placebo, samazināja primārā galarezultāta – fatāla vai nefatāla insulta – risku par 15% (riska attiecība 0,85; 95% ticamības intervāls, 0,72−1,00; p=0,05 vai 0,84; 95% TI, 0,71−0,99; p=0,03 pēc pielāgošanas sākumstāvokļa faktoriem). Kopējā mirstība atorvastatīna grupā bija 9,1% (216/2365), bet placebo grupā – 8,9% (211/2366). Post-hoc analīzē konstatēts, ka 80 mg atorvastatīna, salīdzinot ar placebo, samazina išēmiskā insulta biežumu (218/2365, 9,2% vs 274/2366, 11,6%; p=0,01) un palielina hemorāģiskā insulta biežumu (55/2365, 2,3% vs 33/2366, 1,4%; p=0,02). Hemorāģiskā insulta risks bija lielāks pacientiem, kuri pirms pētījuma bija pārcietuši hemorāģisku insultu (7/45 atorvastatīna grupā, salīdzinot ar 2/48 placebo grupā; RA 4,06; 95% TI, 0,84−19,57), bet išēmiskā insulta risks abās grupās bija praktiski vienāds (3/45 atorvastatīna grupā, salīdzinot ar 2/48 placebo grupā; RA 1,64; 95% TI, 0,27−9,82). Hemorāģiskā insulta risks bija lielāks pacientiem, kas pirms pētījuma bija pārcietuši lakunāru infarktu (20/708 atorvastatīna grupā, salīdzinot ar 4/701 placebo grupā; RA 4,99; 95% TI, 1,71−14,61), vienlaikus šiem pacientiem bija mazāks išēmiskā insulta risks (79/708 atorvastatīna grupā, salīdzinot ar 102/701 placebo grupā; RA 0,76; 95% TI, 0,57−1,02). Iespējams, ka lakunāru infarktu pārcietušiem pacientiem, kuri ārstējas ar 80 mg atorvastatīna dienā, insulta neto risks ir paaugstināts. Pacientu apakšgrupā ar agrāk pārciestu hemorāģisko insultu kopējā mirstība atorvastatīna grupā bija 15,6% (7/45), bet placebo grupā – 10,4% (5/48). Pacientu apakšgrupā ar agrāk pārciestu lakunāru infarktu kopējā mirstība atorvastatīna grupā bija 10,9% (77/708), bet placebo grupā – 9,1% (64/701). (4*) Skatīt – Interpretation of the evidence for the efficacy and safety of statin therapy. In observational studies, blood cholesterol concentrations have been negatively associated with rates of haemorrhagic stroke, particularly at low concentrations of cholesterol in people with high blood pressure. In the randomised SPARCL trial among 4731 patients with prior cerebrovascular disease, allocation to atorvastatin 80 mg daily produced a definite reduction in ischaemic stroke (218 [9·2%] vs 274 [11·6%]; p=0·008), but there was also a possible increase in haemorrhagic stroke (55 [2·3%] vs 33 [1·4%]; p=0·02). When these results were combined with those from the other trials included in the CTT meta-analysis, there was a 21% (95% CI 5–41; p=0·01) proportional increase in the incidence of haemorrhagic stroke per mmol/L reduction in LDL cholesterol. (5*) Simvastatīna zāļu apraksts.
Abās grupās netika novērota nozīmīgas NASP sastopamības atšķirības, salīdzinot 20 mg simvastatīna devu lietošanu (n=1553, 25,7%) ar 80 mg simvastatīna devu lietošanu (n=1447, 24,5%). RA 0,94, 95% TI 0,88–1,01). Pētījuma laikā abās grupās novērotā ZBLH līmeņa absolūtā atšķirība visā pētījumā bija 0,35±0,01 mmol/l. Abās terapijas grupās novērotās drošuma īpašības bija līdzīgas, izņemot miopātijas sastopamību, kas 80 mg simvastatīna devas saņēmušo pacientu grupā bija aptuveni 1,0% pret 0,02% 20 mg saņēmušo pacientu grupā. 20 un 80 mg simvastatīna nozīmīgus asinsvadu sistēmas notikumus ietekmēja vienādi, bet 80 mg grupā 1% lietotāju cieta no miopātijas, bet 20 mg grupā 0,2% lietotāju. Simvastatīna sniegtais ieguvums saistībā ar sirds-asinsvadu notikumiem bērniem ar heFH (iedzimta ģimenes hiperholesterinēmija) nav zināms. (6*) Skatīt šeit. Percent atheroma volume (PAV) 0.99% (95% confidence interval [CI], −1.19 to −0.63) in the atorvastatin group and by 1.22% (95% CI, −1.52 to −0.90) in the rosuvastatin group (P<0.001 for the change from baseline in each group; P=0.17 for the between-group comparison). .. about one third of patients in our study had disease progression despite maximally intensive statin therapy .. Yet intravascular ultrasonography remains a surrogate end point, and a reduction in plaque volume should not be interpreted as equivalent to a clinical benefit in terms of preventing cardiovascular events. .. regression of atherosclerosis was observed in approximately two thirds of the study patients during 104 weeks of statin therapy. For the primary end point (PAV), a numerically higher percentage of rosuvastatin-treated patients had regression (68.5%, vs. 63.2% with atorvastatin). (7*) Pravastatīna zāļu apraksts. Primārā profilakse
Sekundārā profilakse
Pētījumā iekļautiem pacientiem bija arteriālā hipertensija, 40−79 gadus veci, bez miokarda infarkta vai stenokardijas ārstēšanas anamnēzes, ar triglicerīdu līmeni TG ≤6.5 mmol/l (251 mg/dl). Visiem pacientiem bija ne mazāk kā 3 iepriekš definēti riska faktori: vīrieša dzimums, vecums ≥55 gadi, smēķēšana, cukura diabēts, KSS pirmās pakāpes radiniekam, TG:ABL-H >6, perifēro asinsvadu slimība, kreisā kambara hipertrofija, pārciests cerebrovaskulārs notikums, specifiskas EKG pārmaiņas, proteinūrija/ albuminūrija. Ne visiem pacientiem bija augsts pirmreizēja kardiovaskulāra notikuma risks. Pacienti saņēma hipotensīvu terapiju (amlodipīnu vai atenololu) un vai nu atorvastatīnu 10 mg dienā (n=5168), vai placebo (n=5137). Absolūtā un relatīvā riska samazinājums atorvastatīna ietekmē bija šāds: Fatāla koronārā sirds slimība un nefatāls miokarda infarkts 3,3 gadus ilgā novērošanas periodā mazinās 1,1 % zāļu lietotāju. Notikumu skaits (atorvastatīns vs. placebo) 100 vs. 154. Relatīvā riska samazinājums 36%. Atorvastatīna ietekme uz fatālu un nefatālu kardiovaskulāro slimību vērtēta arī randomizētā, dubultaklā, daudzos centros veiktā, placebo kontrolētā pētījumā − Atorvastatīna kolaboratīvā pētījumā diabēta pacientiem (CARDS − Collaborative Atorvastatin Diabetes Study) – kurā bija ietverti pacienti ar 2. tipa cukura diabētu vecumā no 40−75 gadiem bez kardiovaskulāras slimības anamnēzē, kuriem ZBL-H ≤4,14 mmol/l (160 mg/dl) un TG ≤6,78 mmol/l (600 mg/dl). Visiem pacientiem bija vismaz 1 no šādiem riska faktoriem: hipertensija, smēķēšana, retinopātija, mikroalbuminūrija vai makroalbuminūrija. Pacienti vidēji 3,9 gadus lietoja vai nu atorvastatīnu pa 10 mg dienā (n=1428), vai placebo (n=1410). Absolūtā un relatīvā riska samazinājums atorvastatīna ietekmē bija šāds: Nozīmīgi kardiovaskulārie notikumi (fatāli un nefatāli AMI, latenti MI, akūta koronāra nāve, nestabilā stenokardija, koronāro artēriju šuntēšana, perkutānā transluminālā koronārā angioplastija, revaskularizācijas, insulti) mazinājās 3,2% zāļu lietotāju. Notikumu skaits (atorvastatīns vs. placebo) 83 vs. 127. Relatīvā riska samazinājums 37%. All-cause mortality was reduced nonsignificantly by 22% ([−49 to18], P = 0.245) and 37% ([−64 to 9], P = 0.98), respectively. (9*) Fiziski vingrinājumi novērš nāvi 4% sirds mazspējas slimnieku. Exercise training meta-analysis of trials in patients with chronic heart failure (ExTraMATCH). MAIN OUTCOME MEASURE: Death from all causes. RESULTS: During a mean (SD) follow up of 705 (729) days there were 88 (22%) deaths in the exercise arm and 105 (26%) in the control arm. Exercise training significantly reduced mortality (hazard ratio 0.65, 95% confidence interval, 0.46 to 0.92; log rank chi(2) = 5.9; P = 0.015). The secondary end point of death or admission to hospital was also reduced (0.72, 0.56 to 0.93; log rank chi(2) = 6.4; P = 0.011). No statistically significant subgroup specific treatment effect was observed. CONCLUSION: Meta-analysis of randomised trials to date gives no evidence that properly supervised medical training programmes for patients with heart failure might be dangerous, and indeed there is clear evidence of an overall reduction in mortality. Further research should focus on optimising exercise programmes and identifying appropriate patient groups to target. 26%-22% = 4% hronisku sirds mazspējas slimnieku tika novērsta nāve, ja tie iesaistījās fiziskajās aktivitātēs. Physical activity as an index of heart attack risk in college alumni. Fiziska aktivitāte virs 2000 kilokalorijām nedēļā samazina sirdslēkmes risku par 64% (relatīvā riska mazinājums). Kurš profilaktisks kardioloģisks medikaments sola vairāk? Brīdinu, ka nenoskaidroju cik procentiem dalībnieku augstākas aktivitātes grupā mazinājās mirstība. Absolūtā intervences efektivitāte noteikti būs mazāka kā relatīvā, bet relatīvā ir augstāka kā jebkuram statīnam, tāpēc arī absolūtai ir jābūt augstākai. Artis Žeigurs, pediatrs, Latvijas Ārstu biedrības Ētikas komisijas loceklis Publicēts "Latvijas ārsts" 2020. gada jūnijā
Šī ir otrā no divām A. Žeigura sagatavotajām publikācijām. Pirmajā publikācijā viņš analizēja antidepresantu efektivitātes datu nepietiekamo pieejamību pacientiem. Lūdzam apsvērt atbalstu tematiski saistītajai iniciatīvai "Uzrādīt zāļu efektivitāti"! Ja atbalsti šo iniciatīvu, lūdzam ar to dalīties arī ar citiem. Arī sirds un asinsvadu medikamentu efektivitāte tiek turēta noslēpumā24. Nov (2020)
Arī sirds un asinsvadu medikamentu efektivitāte tiek turēta noslēpumā24. Nov (2020)
Piecus gadus lietojot zāles, kopējā mirstība mazinājās 1,8% zāļu lietotāju (14,7 mīnus 12,9).(1*) Tas lektoram būtu kolēģiem jāuzrāda.
Vai statīni ir efektīvs un veselīgs veids kā mazināt holesterīnu un pacientu mirstību?
Pētījumā Study of the Effectiveness of Additional Reductions in Cholesterol and Homocysteine (pētījums par efektivitāti, lai vēl vairāk pazeminātu holesterīna un homocisteīna līmeni) jeb “SEARCH” tika vērtēta terapijas efektivitāte 12'064 pacientiem ar miokarda infarktu anamnēzē, lietojot 80 mg devas un salīdzinot ar 20 mg devu lietošanu (vidējais novērošanas ilgums bija 6,7 gadi) saistībā ar nozīmīgām asinsvadu sistēmas notikumiem (NASP; definētām kā letāla KSS, neletāls MI, koronāras revaskularizācijas procedūra, neletāls vai letāls insults vai perifēra revaskularizācijas procedūra).
West of Scotland Coronary Prevention Study (WOSCOPS)" bija randomizēts, dubultakls, placebo-kontrolēts pētījums, kurā piedalījās 6'595 vīrieši vecumā no 45 līdz 64 gadiem ar mērenu vai smagi izteiktu hiperholesterinēmiju (LDL-holesterīns: 155-232 mg/dl [4,0-6,0 mmol/l]) un bez miokarda infarkta anamnēzē. Viņi tika ārstēti vidēji 4,8 gadus un saņēma 40 mg dienas pravastatīna devu vai placebo papildu diētas pasākumiem.
Samazinājās mirstības risks no koronārās sirds slimības un neletāla miokarda infarkta (relatīvā riska samazinājums (RRR) bija 31%; p = 0,0001 ar absolūto risku 7,9% placebo grupā un 5,5% pacientiem, kuri saņēma pravastatīnu) 2,4% lietotāju (7,9-5,5).
Long-Term Intervention with Pravastatin in Ischemic Diseasei (LIPID) pētījums bija multicentru, randomizēts, dubultakls, placebo kontrolēts pētījums, kura laikā tika salīdzināts pravastatīns (40 mg OD) ar placebo, lietojot vidēji 5,6 gadus 9’014 pacientiem vecumā no 31 līdz 75 gadiem ar normālu un paaugstinātu holesterīna līmeni serumā (sākotnēji kopējais holesterīns = 155 līdz 271 mg/dl [4,0-7,0 mmol/l], vidējais kopējais holesterīns = 219 mg/dl [5,66 mmol/l]), atšķirīgu triglicerīdu līmeni līdz 443 mg/dl [5,0 mmol/l] un miokarda infarktu anamnēzē vai nestabilu stenokardiju iepriekšējos 3 līdz 36 mēnešos.
Ārstēšana ar pravastatīnu ievērojami samazināja relatīvo risku mirstībai no koronārās sirds slimības (KSS) par 24% (p = 0,0004 ar absolūto risku 6,4% placebo grupā un 5,3% pravastatīna grupā) – 1,1% (6,4-5,3).
(8*) Atorvastatīna zāļu apraksts.
Atorvastatīna ietekme uz fatālu un nefatālu koronāro sirds slimību (KSS) vērtēta randomizētā, dubultaklā, placebo kontrolētā pētījumā − angļu-skandināvu kardiālo rezultātu pētījuma lipīdu līmeņa pazemināšanas atzarā (ASCOT-LLA − Anglo-Scandinavian Cardiac Outcomes Trial Lipid Lowering Arm).
Ja pamanījāt kļūdu, lūdzu rakstiet [email protected]![]()
![]()
![]()
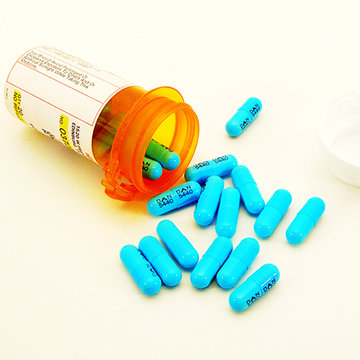 Pārstāvis: Artis ŽeigursPublicēta: 16. May (2019)
Pārstāvis: Artis ŽeigursPublicēta: 16. May (2019)UZRĀDĪT ZĀĻU EFEKTIVITĀTI
Iniciatīva tiks iesniegta Latvijas Republikas Saeimā
Visas zāles neārstē vienlīdz labi. Pārdošanā ir arī tādas, kas palīdz tikai vienam lietotājam no simta, bet pircējs zāļu aprakstā par to netiek brīdināts. Noklusēšana pārkāpj pacienta tiesības uzzināt ārstēšanās izredzes, neļauj salīdzināt un izvēlēties labāko ārstēšanos.
Ar likumu jānosaka pacientiem paredzētajā zāļu aprakstā uzrādīt, cik procentiem lietotāju zāles palīdz katras indikācijas gadījumā, vai arī brīdināt, ja pierādījumu nav.
Saskaņā ar ASV Pārtikas un zāļu pārvaldes datiem mirstība no zāļu blaknēm ir ceturtais biežākais nāves iemesls. Tas liek izvēlēties pēc iespējas efektīvāku un īslaicīgāku ārstēšanos ar zālēm. Pacienti bieži pat neiedomājas, ka pareizās devās un pareizi iedzertas zāles tomēr var nelīdzēt. Iznākumā tas mazina uzticēšanos ārstam. Uzrādīta zāļu efektivitāte novērstu šo pārpratumu. Nemaksājot par maz efektīvām zālēm, vairāk naudas paliks efektīvākām ārstēšanas metodēm. Sirds, asinsvadu, glikozes, tauku vielmaiņas un citu slimību gadījumos 10 tūkstošu soļu noiešana dienā profilaktiski palīdz labāk, nekā daudzas maz efektīvas zāles.
Iniciatīvas jaunumi
Antidepresantu efektivitātes dati pacientiem ir grūti pieejami. Iniciatīvas autors un ārsts Artis Žeigurs vērš ManaBalss kopienas dalībnieku un interesentu uzmanību uz aktuālo jautājumu – pacientu tiesībām uz pilnvērtīgu informāciju par medikamentu efektivitāti. Šī ir pirmā no divām A. Žeigura sagatavotajām publikācijām. Lūdzam apsvērt atbalstu tematiski saistītajai iniciatīvai "Uzrādīt zāļu efektivitāti"! Ja atbalsti šo iniciatīvu, lūdzam ar to dalīties arī ar citiem. Antidepresantu efektivitāte. Kāpēc, izglītojot ārstus, tā būtu jāuzrāda? Vadlīnijās un mūžizglītības lekcijās ārstu izglītotāji neuzrāda cik procentiem lietotāju ieteiktā terapija palīdz. Arī Zāļu valsts aģentūra (ZVA) zāļu efektivitāti neuzrāda. Būtībā – neētiskas ārstu izglītošanas tradīcija turpinās. Bet antidepresanti palīdz līdz trešdaļai zāļu lietotāju, un placebo ir efektīvāks. Kādai pacientu daļai no tiem, kam zāļu grupā stāvoklis uzlabojas, tiešām ir palīdzējušas zāles un kādai – placebo? Placebo kontrolēts pētījums liecina, ka venlafaksīna zāļu grupā pacientiem ar depresiju trauksme mazinās 64,2% lietotāju, bet placebo grupā trauksme mazinās 36,9% lietotāju. Venlafaksīns panāk remisiju 22% lietojāju; palcebo panāk remisiju 26% pacientu. Placebo depresijas ar trauksmi gadījumā attiecīgi ir efektīvāks par zālēm. Preparāta "Venlaxor" zāļu aprakstā nav uzrādīts, cik procentiem lietotāju zāles palīdz. Tā ir steidzami labojama kļūda ZVA darbā. Kāpēc ir svarīgi zināt cik procentiem lietotāju palīdz zāles un cik procentiem lietotāju palīdz placebo? Ja ārstam nav laika uzklausīt un atbalstīt pacientu, tad placebo efekts izpaliks. Zāles palīdzēs ne vairs 64% zāļu lietotāju, bet tikai 27% zāļu lietotāju (64,2% zāļu grupā mīnus 36,9 placebo grupā ir 27,3% zāļu lietotāju, kam palīdz zāles bez placebo). 70 pacientiem no 100 zāles nelīdzēs, un tas ir jāņem vērā, konsultējot depresijas slimnieku. Ārsts nevar steigā izrakstīt antidepresantu un uzskatīt, ka viņš pacientu ir izārstējis. Tiem, kam zāles nelīdz, ir vajadzīgs atkārtots neatliekams veselības stāvokļa novērtējums, placebo un trauksmi mazinoša, terapeitiska saruna. Tāpat arī cilvēciska palīdzība – ģimenes atbalsts, sociālais atbalsts, jurista konsultācija, pašvaldības materiāls atbalsts un apmācība lietās, kas pacientam nesanāk un uztrauc. Cik procentiem lietotāju palīdz citi antidepresanti? Ne vairāk kā trešdaļai. Piemēram, "Citalopram" mazina ģeneralizētu trauksmi 18,6% zāļu lietotāju (zāļu apraksts ZVA mājas lapā). Apvienotie trīs līdzīga plānojuma pētījumu laikā iegūtie dati par 421 pacientu, ko ārstēja ar escitaloprāmu, un 419 pacientiem, kas saņēma placebo, liecina, ka reakcija uz terapiju iestājās attiecīgi 47,5% un 28,9% pacientu (47,5-28,9=18,6). (Skatīt šeit.) Indikācijās depresija, sociālā trauksme, obsesīvi kompulsīvi traucējumi – ZVA efektivitāti nav uzrādījusi, un tā ir steidzami labojama kļūda. Paroksetīns ilgtermiņa depresijas ārstēšanā novērš recidīvus 16% zāļu lietotāju, obsesīvi kompulsīvu traucējumu ārstēšanā – 21% zāļu lietotāju, un panikas ārstēšanā – 25% zāļu lietotāju. Ilgtermiņa efektivitāte Paroksetīna ilgtermiņa efektivitāte depresijas ārstēšanā ir konstatēta 52 nedēļas ilgā uzturošā recidīva profilakses modeļa pētījumā: recidīvs radās 12% pacientu, kuri saņēma paroksetīnu (20-40 mg dienā), salīdzinājumā ar 28% pacientu placebo grupā. Paroksetīna ilgtermiņa efektivitāte obsesīvi kompulsīvu traucējumu ārstēšanā tika pārbaudīta trijos 24 nedēļas ilgos uzturošos recidīva profilakses modeļa pētījumos. Vienā no trim pētījumiem tika panākta būtiska recidīvu skaita atšķirība starp paroksetīna (38%) un placebo grupu (59%). Paroksetīna ilgtermiņa efektivitāte panikas ārstēšanā ir konstatēta 24 nedēļas ilgā uzturošā recidīva profilakses modeļa pētījumā: recidīvs radās 5% pacientu, kuri saņēma paroksetīnu (10-40 mg dienā), salīdzinājumā ar 30% pacientu placebo grupā. To apstiprināja 36 nedēļas ilgs uzturošs pētījums. Paroksetīna ilgtermiņa efektivitāte sociālas neirozes un ģeneralizētas trauksmes, kā arī posttraumatiskā stresa sindroma ārstēšanā nav pietiekami pierādīta. (Skatīt šeit.) Paroksetīna ilgtermiņa efektivitāte sociālas trauksmes un ģeneralizētas trauksmes kā arī posttraumatiskā stresa traucējumu ārstēšanā nav pietiekami pierādīta. Jānorāda, ka 1,27% paroksetīna lietotāju izdara pašnāvību. Klīniskajos pētījumos ar bērniem pastiprināta pašnāvnieciska uzvedība (tajā skaitā pašnāvības mēģinājumi un domas par pašnāvību), paškaitējums un pastiprināts naidīgums tika novēroti vismaz 2% ar paroksetīnu ārstēto pacientu, un to sastopamības biežums bija vismaz divas reizes lielāks nekā placebo grupā (zāļu apraksts ZVA mājas lapā) Blakusparādības, kas novērotas klīniskajos pētījumos bērniem Īslaicīgos (līdz 10-12 nedēļām) klīniskajos pētījumos ar bērniem un pusaudžiem tālāk uzskaitītās blakusparādības tika novērotas vismaz 2% ar paroksetīnu ārstēto pacientu un to biežums bija vismaz divreiz lielāks nekā placebo grupā: pastiprināta suicidāla uzvedība (tai skaitā pašnāvības mēģinājumi un domas par pašnāvību), paškaitējums un pastiprināts naidīgums. Pašnāvības gadījumu analīze pieaugušajiem Specifiska paroksetīna placebo kontrolētu pētījumu analīze pieaugušajiem ar psihiskiem traucējumiem liecināja par palielinātu pašnāvnieciskas uzvedības sastopamību jauniem pieaugušajiem (vecumā no 18 līdz 24 gadiem), kuri ārstēti ar paroksetīnu, salīdzinot ar placebo (2,19% salīdzinājumā ar 0,92%). (Skatīt šeit.) Savukārt vortioksetīns palīdz 15% zāļu lietotāju, bet placebo palīdz 34% pacientu (zāļu apraksts ZVA mājas lapā). Vortioksetīna efektivitāti atbalsta kopējā respondentu analīze, kur vortioksetīna respondentu proporcija bija no 46% līdz 49% pret placebo 34% (p<0,01; NRI analīze). (Skatīt šeit.) Pacientam ir tiesības izvēlēties efektīvāko ārstēšanas metodi, un ārstam ir pienākums to piedāvāt. Par placebo un terapeitisku sarunu. Spriežot pēc antidepresantu pētījumu datiem, depresijas gadījumā placebo un terapeitiska saruna ir efektīvāka par zālēm. Tāpēc ir svarīgi, lai psiholoģiska palīdzība būtu pieejama nekavējoties, un pacientam būtu paredzēts pietiekams laiks sarunai. Lai uzlabotos psihiskās veselības aprūpe valstī, būtu jāpalielina ārstu skaits un vizītes ilgums. ZVA darbs ir steidzami jāuzlabo Daudzos Latvijas ZVA zāļu aprakstos, piemēram, clomipramin un venlaxor, nav uzrādīts, cik procentiem lietotāju zāles palīdz. Tas ir nekavējoties jānovērš. Šīs informācijas trūkums liedz ārstiem un pacientiem uzzināt terapijas paredzamo efektivitāti, kā arī liedz salīdzinot izvēlēties labāko terapiju. Tas rada maldīgu priekšstatu, ka sen reģistrētas vai mazāk pētītas zāles palīdz pilnīgi visiem un ir nekaitīgas. Prakse liecina par pretējo. Uzkrājoties pēcreģistrācijas ziņojumiem, lielākā daļa sen reģistrēto zāļu izrādās mazefektīvas vai pat kaitīgas, un tās ir aizstāj ar labāk pētītām, efektīvākām un nekaitīgākām zālēm. Latvijā ziņošana par neefektivitāti un blaknēm diemžēl īsti nedarbojas, jo kolēģi ziņo maz. Zāļu valsts aģentūra gadā saņem ap 500 ziņojumus. Piemēram, vai antidepresants clomipramine palīdz visiem zāļu lietotājiem? Kā clomipramine salīdzināt ar citiem antidepresantiem un izvēlēties iedarbīgāko, ja nav uzrādīts, cik tas ir efektīvs? Zāļu efektivitāte, tāpat kā blaknes, spriestspējīgam pacientam būtu jāizskaidro. Tas vairo uzticēšanos. Ja medikaments ir augsti efektīvs, tas, visdrīzāk, palīdzēs. Pacients dzers zāles ar prieku, jutīsies labi un slavēs ārstu. Ja medikaments ir mazefektīvs, pacientam tas ir jāzina, lai jau laikus atpazītu neefektivitāti un blaknes un pēc sarunas ar ārstu medikamentu noņemtu vai mainītu. Jo neefektīvu zāļu lietošana ir kaitīga veselībai. Ārsta pienākums ir nekaitēt. Savukārt par neefektivitāti vai blaknēm būtu jāziņo. Tas ir labākais pienesums, ko ikviens pacients var dot veselības aprūpes uzlabošanā. Nav cita veida, kā iegūt un apkopot zāļu aprakstā ticamu informāciju par zālēm. Kā mediķiem, tā pacientiem ir jāapzinās, ka zāles nenovērš depresiju veicinošus apstākļus – psihotraumējošus notikumus un atkarības un nemāca veselīgu dzīvesveidu. Tās nepalīdz uzlabot attiecības ģimenē un atrast piemērotu darbu. Tās nemāca atrast vaļasprieku un cerīgi skatīties nākotnē. Depresiju mazina izprasts terapijas plāns, pacienta apmācība un sociālais atbalsts. Lai iegūtu pacienta uzticību, ir nepieciešams laiks sarunai. Bez savstarpējas uzticēšanās un izpratnes par ārstēšanu arī placebo nedarbojas, un pacienta līdzestība ir zema. (Līdzestība ir skatījumu uz pacientu kā informētu, mērķtiecīgu un neatlaidīgu ārstniecības procesa dalībnieku. Angliski "līdzestība" – compliance, adherence. Avots – šeit.) Veselības aprūpes organizatoriem depresijas gadījumā ir jāapmaksā efektīvākā ārstēšana – laiks pacienta un ārsta izsmeļošai sarunai par nepieciešamajām izmaiņām dzīvesveidā un uzskatos, kā arī pacientam ir jānodrošina sociālais atbalsts. Bez pietiekama laika sarunai efektīvākā ārstēšana – placebo – nedarbojas, tāpēc arī pacienta veselības aprūpe kļūst neefektīva. Un ZVA noteikti ir jāuzrāda, cik procentiem lietotāju zāles palīdz. Tas ir jānorāda arī ārstēšanas vadlīnijās. Artis Žeigurs, pediatrs, Ārstu Ētikas komisijas loceklis Publikācija par šo ir lasāma arī žurnālā "Latvijas ārsts" 2020. gada septembrī. Ja pamanījāt kļūdu, rakstiet [email protected]! Tiesības zināt: zāļu efektivitāte09. Nov (2020)
Tiesības zināt: zāļu efektivitāte09. Nov (2020)![]()
![]()
![]()









 English
English Latviski
Latviski




